Катализаторы. Старт в науке Каталитическое восстановление водородом
Под процессами прямого восстановления железа понимают такие процессы, которые дают возможность получать непосредственно из руды металлическое железо, минуя доменную печь. Способы прямого получения железа позволяют вести процесс не расходуя металлургический кокс, заменяя его другими видами топлива.
Известно, что использование железа прямого восстановления при выплавке стали (в основном, в электродуговых печах) позволяет производить наиболее высококачественный, экономически выгодный (с относительно низкой энергоемкостью) и экологически чистый металл без примесей серы и фосфора, пригодный для удовлетворения самых высоких требований таких отраслей-потребителей, как машиностроение (авиа-, судостроение и т. д.). В настоящее время предложено более 20 различных способов прямого получения железа.
Железо прямого восстановления (или губчатое железо) в основном производят в виде металлизированных окатышей: холодных СDRI (Сool Direct Reduced Iron) или горячих HDRI (Hot Direct Reduced Iron), а также горячебрикетированного железа НBI (Hot Briquetted Iron).
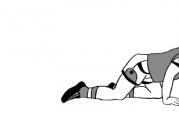
Рис.38. Внешний вид железа прямого восстановления СDRI (а),HDRI (б) и НBI (в)
Окатыши СDRI (рис. 38 а) получают в основном в шахтных печах с охлаждением в нижней части печи до 50º С, после чего отравляются на склад, а затем загружаются в электропечь.
Окатыши HDRI (рис. 38 б) выгружаются из установки прямого восстановления в горячем состоянии и загружаются в расположенную рядом электропечь при температуре 600º С и выше.
Горячебрикетированное железо НBI (рис. 38 в) получается путем прессования брикетов размерами 30×50×110 мм в формы в виде подушек из металлизированного продукта, который выгружается из печи при температуре около 700º С.
Наибольшее распространение получили технологии компании Midrex (США). Процесс протекает в шахтной печи, в верхнюю часть которой подаются окатыши или кусковая руда. Установки Midrex действуют на многих предприятиях крупнейшей металлургической компании ArcelorMittal, расположенных в Германии, Канаде, Мексике, Тринидаде и Тобаго и ЮАР.
Второй по распространенности технологией прямого восстановления железа является HYL/Energiron. Процесс HYL был разработан мексиканской компанией Tenova для прямого восстановления железной руды (кусковой или окатышей) в металлическое железо с помощью восстановительного газа в реакторе с подвижным слоем.
Менее известна технология Finmet, которая позволяет использовать железорудную мелочь без предварительного окускования в процессе газового восстановления в кипящем (псевдосжиженном) слое. По этой технологии пока действует только одно предприятие — Orinoco Iron в Венесуэле.
Для получения железа прямого восстановления также применяется целый ряд угольных технологий — SL/RN, Jindal, DRC, SIIL, Tisco, Codir и др. В основном все они действуют на базе печей с вращающимся подом с использованием угля или пылеугольной смеси.
Такие предприятия работают в Индии, а также в ЮАР, Китае, Перу и в некоторых других странах. Хотя экологичность таких производств и качество получаемого металла существенно ниже, чем у «газовых» предприятий, однако они дешевле, что и обеспечивает им значительную долю в структуре мирового производства DRI.
Существуют также жидкофазные способы прямого восстановления и альтернативные доменной печи установки для получения чугуна.
 Рис. 39. Доля способов производства железа прямого восстановления в мире
Рис. 39. Доля способов производства железа прямого восстановления в мире
Структура производства железа прямого восстановления в мире в последние годы приведена на рис. 39.
Производство железа в шахтных печах (технология Midrex)
В шахтных печах получают губчатое железо газообразными восстановителями в толстом слое железосодержащих окатышей. Схема производства различных видов железа прямого восстановления с использованием шахтной печи приведена на рис. 40.
 Рис. 40. Технологическая схема производства железа прямого восстановления в шахтных печах
Рис. 40. Технологическая схема производства железа прямого восстановления в шахтных печах
Процесс производства железа осуществляют в противотоке железорудных материалов, загружаемых в агрегат сверху, и нагретых восстановительных газов, подаваемых снизу. Работа агрегата в противотоке дает возможность достигать высокой производительности при хорошем использовании газа.
В качестве восстановителей применяют конвертированный природный газ, состоящий в основном из водорода (H 2) и оксида углерода (CO). Восстановительный газ получают в кислородном реакторе (реформере), путем неполного сжигания природного газа в кислороде. Полученный газ, содержащий 29% CO, 55% H 2 и 13% окислителей (H 2 O и CO 2) освобождают частично от окислителей, затем нагревают, до температуры 1100…1150 °С и через фурмы подают в печь.
Добытую руду обогащают и получают окатыши. Окатыши из бункера загружают в шахтную печь, работающую по принципу противотока. Для восстановления железа из окатышей в среднюю часть печи по трубопроводу подают конвертированный природный газ. В восстановительной зоне печи создается температура 1000…1100 °C, при которой H 2 и CO восстанавливают железную руду в окатышах до твёрдого губчатого железа. Содержание железа в окатышах достигает 90…95%. Для охлаждения железных окатышей, снизу печи в зону охлаждения печи подают воздух. Охлаждённые окатыши выдаются на конвейер и поступают на выплавку стали в электропечах. Если производятся горячие окатыши или горячебрикетированное железо, то охлаждение восстановленного железа в нижней зоне печи не производится.
Производство железа в периодически действующих ретортах (технология HYL/Energiron)
Еще одним способом производства железа прямого восстановления является процесс в периодически действующих ретортах, используемых в качестве агрегатов восстановления. На установке таких реторт четыре (рис. 41). Емкость каждой реторты 100…150 т.
 Рис. 41. Схема установки HYL: 1 – десульфуратор природного газа; 2 – установка конверсии; 3 – котел-утилизатор; 4 –
Рис. 41. Схема установки HYL: 1 – десульфуратор природного газа; 2 – установка конверсии; 3 – котел-утилизатор; 4 –барабан для производства пара; 5 – воздушный охладитель; 6 – воздуходувка; 7 – скруббер; 8 – воздухонагреватель; 9 – загрузочный бункер; 10 – нагреватель газа; 11 – реторты (I – IV); 12 – скруббер; 13 – конвейер подачи руды; 14 – конвейер уборки губчатого железа; 15 – сборный бункер губчатого железа
Реторты переставляются с одной позиции на другую, что обуславливает циклический характер процесса, состоящего из последовательных операций загрузки, нагрева и восстановления шихты, охлаждения и выгрузки губчатого железа. Реторты загружают и подают газ сверху. В качестве сырья используют чистые руды, содержащие не менее 60 % железа, крупностью 12…50 мм.
Восстановление ведется в неподвижном слое кусковой руды или окатышей при избыточном давлении 0,35…0,4 МПа и температуре 870…1040 °С. Нагрев руды и компенсация тепловых потерь процесса осуществляют за счет физического тепла восстановительного газа, который нагревают до 980…1240 ºС. При выдержке 4…6 часов средняя степень металлизации железа составляет 85 %. Выгрузку губчатого железа производят снизу с помощью специальных скребков. Губчатое железо поступает на конвейер транспортирующий губку в сталеплавильное отделение. На рис. 42 показана схема стационарной реторты со съемной крышкой и откидным днищем.
 Рис. 42. Конструкция реторты: 1 – гидравлический цилиндр; 2 – тележка; 3 – привод; 4 – кожух; 5 – крышка; 6 – загрузочная
Рис. 42. Конструкция реторты: 1 – гидравлический цилиндр; 2 – тележка; 3 – привод; 4 – кожух; 5 – крышка; 6 – загрузочнаягорловина; 7 – площадка для обслуживания; 8 – резец с рычагом
для удаления губчатого железа; 9 – губчатое железо; 10 – футеровка; 11 – механизм управления откидным днищем; 12 – откидное днище; 13 – разгрузочный желоб
В каждой из четырех реторт протекают различные процессы. В одной реторте происходит предварительный нагрев и восстановление шихты газом, выходящим из других реторт. В двух ретортах происходит довосстановление железа подогретым газом, получаемым в конверсионной установке. В четвертой происходит науглероживание губчатого железа. Готовое железо поступает на конвейер, а в освобожденную реторту загружают исходную шихту.
К недостаткам метода относят:
- периодичность процесса;
- неравномерность металлизации по высоте;
- низкая степень металлизации в сравнении с процессами, осуществляемыми в шахтных печах.
Производство железа на движущейся колосниковой решетке
Процесс получения железа на движущейся колосниковой решетке (рис. 43) несколько напоминает работу агломерационной машины. В этом случае конвертируемый газ проходит сверху вниз через слой шихты.
 Рис. 43. Схема процесса получения железа на движущейся колосниковой решётке: 1 – обжиговая конвейерная машина, 2 – шихта, 3 – зона сушки, 4 – зона обжига и восстановления, 5 – электропечь, 6 – ковш для жидкого металла, 7 – ковш для шлака
Рис. 43. Схема процесса получения железа на движущейся колосниковой решётке: 1 – обжиговая конвейерная машина, 2 – шихта, 3 – зона сушки, 4 – зона обжига и восстановления, 5 – электропечь, 6 – ковш для жидкого металла, 7 – ковш для шлака
Существует разновидность процесса получения железа на движущейся колосниковой решетке, когда вместо конвертированного газа используют твердый восстановитель (каменный уголь, кокс и т.д.).
В этом случае сырые окатыши в головной части установки сушат рециркулируемыми газами, после чего окатыши поступают в зону обжига, где в результате просасывания горячих газов происходит нагрев и восстановление оксидов железа. Основным преимуществом этого процесса является возможность подавать в установку для восстановления неупрочненные обжигом окатыши. Недостатком этого процесса является загрязнение губчатого железа пустой породой, серой и фосфором твердого топлива.
Производство железа во вращающихся трубчатых печах
Другой разновидностью процесса с использованием твердого восстановителя является способ получения железа во вращающихся трубчатых печах (рис. 44).
 Рис. 44. Схема установки с применением трубчатых вращающихся печей: 1 – элеватор; 2 – исходная шихта; 3 – вращающаяся печь; 4– вибропитатель; 5 – пылеуловитель; 6 – уборка пыли; 7 – зона горения топлива и плавления материалов; 8 – горелка
Рис. 44. Схема установки с применением трубчатых вращающихся печей: 1 – элеватор; 2 – исходная шихта; 3 – вращающаяся печь; 4– вибропитатель; 5 – пылеуловитель; 6 – уборка пыли; 7 – зона горения топлива и плавления материалов; 8 – горелка
По этому способу во вращающуюся трубчатую печь, установленную под небольшим углом к горизонту, загружается шихта, состоящая из руды, твердого топлива и доломита или известняка. Доломит и известняк используются для десульфурации. Печь отапливается газообразным или жидким топливом при помощи горелок, установленных на разгрузочном конце печи.
По мере продвижения шихты от загрузочного конца печи к разгрузочному, навстречу газообразным продуктам горения, происходит восстановление оксидов железа. Восстановление протекает в основном через газовую фазу при участии твердого углерода. На разгрузочном конце печи восстановленный материал для предупреждения окисления охлаждается в специальном вращающемся охладителе и после дробления и последующего магнитного обогащения используется в сталеплавильном производстве.
Производство железа в реакторах кипящего слоя
В основу этого способа положен эффект так называемого кипящего слоя, при котором создаются условия для хорошего контакта мелких железорудных материалов с газообразным восстановителем.
Сущность явления кипящего слоя заключается в следующем. Если через слой зернистого материала пропускать восходящий поток газа, то при небольших скоростях газа твердые частицы будут оставаться неподвижными. Слой будет выполнять роль фильтрующего пористого элемента.
Для создания кипящего слоя под горизонтальную решетку реактора, на которую загружают исходный железорудный материал, подается горячий восстановительный газ с определенной скоростью.
Чтобы предотвратить спекание восстановленного железа процесс ведется при низкой температуре (около 500 °С). Железо полученное при этой температуре, характеризуется повышенной пирофорностью (самовозгораемостью на воздухе). Для предотвращения пирофорности полученное железо нагревают до 820…880 °С с последующим охлаждением в восстановительной или нейтральной атмосфере.
Агрегаты FASTMET и ITmk3
В данных агрегатах осуществляется получение железа из руды и некосующегося угля. В агрегатах FASTMET также могут утилизироваться побочные продукты (пыли и шламы), содержащие железо, которые образуются на заводах с полным металлургическим циклом. Развитие этой технологии привело к созданию в 1996 г. процесса ITmk3 производства «передельного чугуна высшего качества» из окатышей или брикетов, схема процессов приведена на рис. 45.
 Рис. 45. Схема процессов FASTMET, FAST MELT и ITmk3:1-бункера с компонентами шихты; 2 — окомкование; 3 —
Рис. 45. Схема процессов FASTMET, FAST MELT и ITmk3:1-бункера с компонентами шихты; 2 — окомкование; 3 —сушка; 4 — брикетирование; 5 — печь с вращающимся подом; 6 — компрессор; 7 – регенератор; 8 – воздух для горелки; 9 – топливо для горелки; 10 – газоочистка; 11 – дымовая труба; 12 — электросталеплавильная печь; 13 – сепаратор
Технология получения железа следующая. Из мелкой железной руды после ее смешивания с углем получают гранулы, которые высушивают и загружают в печь с вращающимся подом. Процесс по существу выполняется на большом поворотном столе, который вращается в пределах тороидального огражденного пространства.
Гранулы из шихты загружаются на вращающийся под печи одним или двумя слоями и во время вращения нагреваются горелками, расположенными над слоем, где также происходит дожигание оксида углерода и летучих угля, выделяющихся при нагреве и восстановлении оксидов. Один оборот вращающейся печи осуществляется за 10 мин.
В случае процесса FASTMET продукцией является губчатое железо, FASTMELT – жидкая сталь, а в процессе ITmk3 данные комки плавятся в последней зоне этого пода, тем самым получая гранулы чугуна и шлак. Конечным этапом является разделение чугунных комков и шлака.
Химико-термический способ получения железа
Данный метод применяется для получения очень чистого железа из труднообогатимого рудного сырья, содержащего большое количество вредных примесей. Он может быть использован также для получения легированной железной губки из комплексных руд.
Схема технологического процесса получения железа по этому методу включает следующие операции (рис. 46).
 Рис. 46. Схема технологического процесса прямого получения железа химико-термическим способом: 1 – печь восстановительного обжига; 2 – реакторы растворения; 3, 5 – промежуточные ёмкости; 4 – фильтры; 6 – выпарные аппараты; 7 – кристаллизаторы; 8 – центрифуга; 9 – вакуум-сушилка; 10 – печь сушки хлоридов; 11 – печь окисления хлоридов; 12 – гранулятор; 13 – печь восстановления хлоридов
Рис. 46. Схема технологического процесса прямого получения железа химико-термическим способом: 1 – печь восстановительного обжига; 2 – реакторы растворения; 3, 5 – промежуточные ёмкости; 4 – фильтры; 6 – выпарные аппараты; 7 – кристаллизаторы; 8 – центрифуга; 9 – вакуум-сушилка; 10 – печь сушки хлоридов; 11 – печь окисления хлоридов; 12 – гранулятор; 13 – печь восстановления хлоридов
Усредненная на рудном дворе руда поступает в дробильное отделение, а затем в печь обжига. Для ускорения процесса обжиг руды проводится с использованием твердого восстановителя. Для этого приёмные бункеры мельниц оборудуются дозаторами для приготовления шихты, состоящей из руды и твердого восстановителя.
Подготовленная шихта поставляется в печь для восстановительного обжига. Обжиг проводится при температуре 900…1000 °С. После обжига руда поступает в реакторы растворения руды, заполненные соляной кислотой. Начальная стадия растворения происходит очень бурно и сопровождается выделением водорода. По мере снижения концентрации кислоты и сокращения поверхности твердой фазы скорость реакции растворения падает. Для ускорения процесса на конечном этапе реакционный объём подогревается паром с температурой 80…90 °С, подаваемом в паровые рубашки реакторов.
Выделяющийся при растворении водород после очистки направляется в печь восстановления хлоридов, где используется как газообразный восстановитель. Пары соляной кислоты, сконденсировавшиеся в процессе растворения, поступают в систему сбора кислоты, откуда направляются в реактор растворения.
Полученная в результате растворения пульпа подаётся в фильтры для отделения раствора от нерастворимого остатка. Отфильтрованный раствор поступает в выпарные аппараты, где проводится выпаривание до насыщения по хлористому железу. Далее раствор направляется в кристаллизаторы, из которых смесь кристаллов и раствора подается на центрифуги. Из центрифуг кристаллы направляются в печь сушки и затем в печь восстановления хлоридов, отапливающуюся природным газом.
Для восстановления хлоридов используется водород. Температура восстановления составляет 600…700 °С. В результате, после восстановления, образуется химически чистое железо.
Отходящий из печей газ, содержащий водород и пары воды, подвергается осушке, очистке и используется как восстановитель при восстановлении хлоридов. Кислота, образующаяся в результате охлаждения и очистки отходящих газов, поступает в систему сбора соляной кислоты, откуда направляется в реакторы растворения руды.
Таким образом, процесс построен максимально рационально, поскольку обеспечивается рециркуляция всех реагентов, участвующих в процессе.
А) Железо в присутствии электролитов - восстанавливает ароматические нитросоединения до соответствующих аминов (один из распространенных промышленных методов). При этом одновременно протекает четыререакции :
Скорость процесса восстановления лимитируется первой стадией, которая аналогична процессу влажной коррозии железа. Поэтому восстановление ведут в средеэлектролита , как правило,в слабокислой среде . При повышении величинырН среды скорость реакции уменьшается. При рН > 12 процесс практически прекращается.
Электролиты вводят в реакционную массу в готовом виде (хлорид аммония) или получают в самом реакторе при протравливании чугунной стружки соляной кислотой. Наиболееактивным электролитом является хлорид аммония,менее активным хлорид железа (II), сульфат аммония и т.д.
Для восстановления лучше всего использовать стружку серого чугуна , которая является отходом металлообрабатывающих производств.Активность серого чугуна объясняется возникновением в присутствии электролитов гальванической пары на границе раздела: железо - графит. Вследствие зернистого строения серый чугун в процессе восстановления распадается на мелкие частицы, что ведет к ускорению реакции.
Чугунная стружка должна быть специально подготовлена для реакции. После измельчения и просева, а также удаления пыли, чугунную стружку обезжиривают и протравливают небольшим количеством соляной кислоты, что увеличивает ее активность вследствие образования хлоридов.
Процесс восстановления чугунной стружкой ведутпри температуре кипения реакционной массы . Обогрев чаще всего производят острым паром.
Обычно к нагретой до температуры кипения суспензии чугунной стружки в растворе электролита постепенно загружают нитропродукт. Каждую следующую порцию вводят лишь после того, как прореагирует предыдущая. В некоторых случаях порядок загрузки может быть изменен.
Если получающийся амин летуч с водяным паром, то часть его отгоняется во время процесса с водяным паром. Смесь паров воды и амина конденсируется в холодильнике, после чего поступает в отстойник для разделения. Остальную часть амина отгоняютс водяным паром после окончания процесса восстановления и подщелачивания реакционной массы. Иногда предварительно выделившийся амин сифонируют после отстаивания реакционной массы в редукторе. Амины, плохо перегоняющиеся с водяным паром,экстрагируют из реакционной массы органическими растворителями.
В производстве восстановление проводят в стальных или чугунных аппаратах (редукторах ), футерованных диабазовой плиткой на кислотоупорной замазке и снабженных мешалкой (лопастной или сошниковой) и барботером для подачи острого пара.
Этот метод используют при производстве анестезина, новокаина, дифенилсульфона и ряда других препаратов:
Достоинства метода : простота технологии, дешевизна сырья, высокий выход целевого продукта реакции.Недостатки : сокращение сырьевой базы и нестабильное качество чугунной стружки; трудности по утилизации образующегося шлама (фильтрация, транспортировка плохо фильтрующегося тяжелого и содержащего абразивные частицы осадка).
Б ) Железные опилки в среде соляной или уксусной кислот - восстанавливают нитросоединения , азосоединения и альдегиды .

Процесс ведут при температуре кипения, медленно добавляя нитросоединение к суспензии железа в слабокислой водной или водно-спиртовойсреде . Концентрация спирта может иметь большое значение. Наилучшие результаты получают при работе сжелезом , восстановленным водородом. Добавление небольшого количествахлорида никеля ускоряет реакцию.
В) Сульфат железа (II ) в присутствии аммиака - восстанавливает нитрогруппу в молекулах соединений, содержащих и другие способные к восстановлению группы. Этот метод дает хорошие результаты при восстановлении ароматических нитрокарбоновых кислот и нитроальдегидов.
§ 24. Определение соединений железа (III)
Определение соединений железа (III) перманганатометрическим методом основано на предварительном восстановлении до соответствующим восстановителем и последующем титровании железа (II) стандартным раствором перманганата.
Восстановление железа (III) до железа (II) может быть проведено цинком, алюминием, висмутом, хлоридом олова (II), жидкими амальгамами и др. Из металлов чаще всего пользуются гранулированным цинком, цинковой пылью или амальгамированным цинком. Восстановление металлическим цинком или амальгамированным цинком целесообразно проводить при отсутствии в анализируемом растворе других ионов, способных восстанавливаться (например, титана, ванадия, хрома, молибдена и т. п.).
Восстановление соединений железа (III) хлоридом олова (II). Иногда -ионы восстанавливают хлоридом олова (II):
Избыток хлорида олова (II) окисляют прибавлением хлорида ртути (II):
Образующаяся каломель при титровании железа (II) перманганатом окисляется очень медленно и не мешает определению.
Восстановление соединений железа (III) металлическим цинком. При восстановлении цинком рассчитанную навеску соли железа (III) помещают в круглодонную колбу, в которую прибавляют разбавленной ( серной кислоты; затем в колбу высыпают рассчитанное (с большим избытком) количество цинковой пыли или стружек. Колбу закрывают пробкой, снабженной клапаном Бунзена (рис. 54) и нагревают на водяной бане до полного растворения цинка. Колбу устанавливают косо во избежание разбрызгивания. После растворения цинка раствор охлаждают и количественно переносят в мерную колбу, перемешивают и титруют перманганатом.
Восстановление соединений железа (III) амальгамированным цинком (в редукторе Джойса). Редуктор Джонса (рис. 55) представляет собой стеклянную трубку длиной 25-30 см и внутренним диаметром см. В верхней части трубка имеет расширение емкостью . В нижней части трубка сужена и снабжена стеклянным краном, как бюретка. Приемником служит коническая колба. Если восстановленный раствор легко окисляется воздухом, то колбу закрывают пробкой с двумя отверстиями, через одно из которых проходит трубка редуктора (при титровании заменяется бюреткой), через другое - трубка, через которую колбу можно наполнить двуокисью углерода.
Примечание. Если восстановление вести при доступе воздуха, то образуется перекись водорода, которая восстанавливает окислитель при последующем титровании восстановителя.
В нижнюю часть редуктора помещают дырчатую фарфоровую пластинку, пористую стеклянную пластинку или несколько стеклянных шариков, на которые положен слой стеклянной ваты. На фильтрующий слой помещают кусочки (величиной мм) амальгамированного цинка.
Цинк амальгамируют обработкой раствором хлорида окисной ртути , для чего 200 г цинка высыпают в -ного раствора хлорида окисной ртути, перемешивают 5-6 мин и промывают декантацией горячей водой.
Для зарядки редуктор сначала наполняют дистиллированной водой и затем осторожно насыпают в него цинк, следя за тем, чтобы в слой металла не попали пузырьки воздуха. Высота слоя цинка 20-25 см. Верхний слой металла всегда должен быть покрыт водой.
Катализ
- избирательное ускорение одного из возможных термодинамически разрешенных направлений химической реакции под действием катализатора, который многократно вступает в промежуточное химическое взаимодействие с участниками реакции и восстанавливает свой химический состав после каждого цикла промежуточных химических взаимодействий.
Иными словами, суть катализа состоит в изменении скоростей химических реакций при действии катализаторов.
Катализатор
– вещества, изменяющие скорость химической реакции или вызывающие её, но НЕ входящие в состав продуктов.

Катализаторы подразделяются на гомогенные
и гетерогенные
. Гомогенный катализатор
находится в одной фазе с реагирующими веществами, гетерогенный - образует самостоятельную фазу, отделённую границей раздела от фазы, в которой находятся реагирующие вещества. Типичными гомогенными катализаторами являются кислоты и основания. В качестве гетерогенных катализаторов применяются металлы, их оксиды и сульфиды.
Реакции одного и того же типа могут протекать как с гомогенными, так и с гетерогенными катализаторами. Так, наряду с растворами кислот применяются имеющие кислотные свойства твёрдые Al 2 О 3 , TiO 2 , ThO 2 , алюмосиликаты, цеолиты. Гетерогенные катализаторы с основными свойствами: CaО, BaО, MgО.
Гетерогенные катализаторы
имеют, как правило, сильно развитую поверхность, для чего их распределяют на инертном носителе (силикагель, оксид алюминия, активированный уголь и др.).
Гетерогенные катализаторы редко применяются в виде индивидуальных веществ и, как правило, содержат носитель и различные добавки, получившие название модификаторов. Цели их введения разнообразны: повышение активности катализатора (промоторы), его избирательности и стабильности, улучшение механических и структурных свойств. Фазовые и структурные модификаторы стабилизируют соответственно активную фазу и пористую структуру поверхности катализатора.
В смешанных катализаторах, где компоненты находятся в соизмеримых количествах (например, в алюмокобальт- или алюмоникельмолибденовых катализаторах процессов гидроочистки нефтяного сырья), могут образоваться новые, более активные соединения, их твердый раствор в основном компоненте или же многофазные системы, обладающие специфическим каталитическим действием. Так, Со или Ni в отдельности обладают высокой де- и гидрирующей активностью, но исключительно чувствительны к отравляющему действию сернистых соединений. Мо в отношении этой реакции малоактивен, но обладает большим сродством к сернистым соединениям. Катализаторы, в которых одновременно присутствуют Мо и Со или Ni в оптимальных соотношениях, весьма эффективны в реакциях гидрогенолиза сернистых и других гетероорганических соединений нефтяного сырья.
Не менее важна роль носителей гетерогенных катализаторов, особенно в случае дорогостоящих металлических катализаторов (Pt, Pd, Ni, Со, Ag). Подбором носителя достигаются требуемые пористая структура, удельная поверхность, механическая прочность и термостойкость. В качестве носителей используют окиси алюминия, алюмосиликаты, окиси хрома или кремния, активированный уголь, пемзу, кизельгур и другие природные и синтетические материалы. Особый класс представляют цеолитсодержащие алюмосиликатные катализаторы крекинга нефтяного сырья. Главную роль в них играют кристаллические цеолиты, имеющие каркасную структуру с относительно большими сотообразными полостями, которые сообщаются окнами малых размеров, связывающими полости между собой. В 1 г цеолита имеется около 1020 полостей и 800 м2 поверхности, способной к ионному обмену на металлы. Цеолиты диспергируются в аморфной матрице, которая выполняет роль носителя с крупными порами и при крекинге способствует первичному распаду высокомолекулярного нефтяного сырья и тем самым готовит сырье для последующих вторичных реакций на цеолите.

Исходя из изложенного выше, можно сделать вывод, что промышленные катализаторы состоят из: матрицы
(носителя
), активного компонента
и вспомогательных добавок
или присадок
. В зависимости от механизма взаимодействия нанесенные катализаторы бывают «сорбционными» и «пропиточными».
«Сорбционные» – в процессе приготовления имеет место взаимодействие между носителем и исходным веществом, адсорбирующимся на поверхности.
«Пропиточные» – такое взаимодействие практически отсутствует и исходное соединение активного компонента находится в растворенном состоянии в порах носителя.
Характерное свойство нанесённых катализаторов – неравномерность распределения активного компонента по сечению гранулы. Четыре основных типа: I – с равномерным распределением; II – «корочковый», у которых активный компонент сосредоточен у периферии гранул; III – активный компонент сосредоточен в центре гранулы («яичный желток»); IV – активный компонент расположен в средней области, удаленной как от центра, так и от внешней поверхности зерна катализатора.

Матрица должна обеспечивать сохранение каталитических свойств катализатора в условиях высоких температур, предохранять его от воздействия каталитических ядов, создавать определенную форму, гранулометрический состав и необходимую механическую прочность частиц, обеспечивать доступность активных металлов для молекул сырья. Вещество матрицы способствует равномерному распределению активных металлов в порах катализатора и интенсивному протеканию массо- и теплообменных процессов. Оно существенно влияет на термическую стабильность катализатора.

Основными технологическими характеристиками катализаторов являются активность и селективность (избирательность) по отношению к данной реакции, стабильность и регенерируемость, а также гранулометрический состав, плотность, механическая прочность на раздавливание и истирание.
Активность катализатора
– определяется удельной скоростью данной каталитической реакции, т. е. количеством продукта, образующегося в единицу времени на единицу объёма катализатора или реактора. Количественно активность определяют как скорость реакции в данных условиях за вычетом скорости той же реакции в отсутствие катализатора. Потеря активности катализатора происходит, главным образом, в результате отложений кокса на поверхности и в порах его носителя.
Активные центры гетерогенного катализатора
– специфические центры на поверхности твёрдого тела (или макромолекулы), при взаимодействии с которыми молекулы реагирующего вещества активируются и реакция протекает с большей скоростью (каталитически активной является не вся поверхность гетерогенного катализатора, а лишь некоторые участки её
). В гомогенном катализе в идеальном случае все молекулы растворенного катализатора являются АЦ и образуют с реагентами промежуточные реакционноспособные продукты.
В подавляющем большинстве случаев в присутствии данного катализатора, помимо основной реакции, протекает еще ряд побочных параллельных или последовательных реакций. Доля прореагировавших исходных веществ с образованием целевых продуктов характеризует селективность
катализатора. Она зависит не только от природы катализатора, но и от параметров каталитического процесса, поэтому ее следует относить к определенным условиям проведения реакции. Селективность зависит также от термодинамического равновесия. В нефтепереработке иногда селективность условно выражают как отношение выходов целевого и побочного продуктов, например таких, как бензин/газ, бензин/кокс или бензин/газ + кокс.

Стабильность
является одним из важнейших показателей качества катализатора, характеризует его способность сохранять свою активность во времени. От нее зависят стабильность работы установок, продолжительность их межремонтного пробега, технологическое оформление, расход катализатора, материальные и экономические затраты, вопросы охраны окружающей среды и технико-экономические показатели процесса и др.
В процессе длительной эксплуатации катализаторы с определенной интенсивностью претерпевают физико-химические изменения, приводящие к снижению или потере их каталитической активности (иногда селективности), т. е. катализаторы подвергаются физической и химической дезактивации.
Физическая дезактивация (спекание)
катализатора происходит под воздействием высокой температуры (в некоторых каталитических процессах) и водяного пара и при его транспортировке и циркуляции. Этот процесс сопровождается снижением удельной поверхности как носителя (матрицы) катализатора, так и активного компонента (в результате рекристаллизации - коалесценции нанесенного металла с потерей дисперсности).
Химическая дезактивация
катализатора обусловливается:
отравлением его активных центров некоторыми содержащимися в сырье примесями, называемыми ядом (например, сернистыми соединениями в случае алюмоплатиновых катализаторов риформинга);
блокировкой его активных центров углистыми отложениями (коксом) или металлоорганическими соединениями, содержащимися в нефтяном сырье.
В зависимости от того, восстанавливается или не восстанавливается каталитическая активность после регенерации катализатора, различают соответственно обратимую и необратимую дезактивации. Однако даже в случае обратимой дезактивации катализатор в конечном счете «стареет» и приходится выгружать его из реактора.
Большое влияние на промышленные процессы оказывает механическая прочность
катализатора. Так на всех современных установках каталитического крекинга использован принцип непрерывного движения катализатора - в виде псевдоожиженного слоя, по линии пневмотранспорта или реже в виде слоя крупногранулированных частиц. Во всех случаях частицы претерпевают трение и удары о стенки аппаратуры и друг о друга, в результате чего они могут раскалываться или истираться. Образование катализаторной крошки и пыли нарушает режим пневмотранспорта и псевдоожижения, увеличивает перепад давления в линии. Образующиеся пыль и крошку удаляют, поэтому необходимо заменять их свежими порциями катализатора, что повышает расходы на эксплуатацию установки. Механическую прочность катализаторов определяют методом истирания проб в циркуляционной системе - в псевдоожиженном слое, с одновременными ударами частиц о металлическую поверхность и др.
Еще одной характеристикой катализатора является его регенерируемость
. Под регенерируемостью катализатора понимается как способность его восстанавливать активность после соответствующей обработки, так и количественные характеристики процесса регенерации, прежде всего его скорость.
Большое влияние на качество катализатора оказывает способ его получения. Поскольку каталитическая реакция протекает на поверхности, целесообразно получить катализатор с максимально развитой поверхностью с большим количеством пор. Для разных реакций оптимальными могут быть узкие или, наоборот, более широкие поры, а также их комбинации. Не менее важны форма и размер зерен катализатора - от этого зависят удельная производительность, гидравлическое сопротивление слоя катализатора и конструкция реакционных аппаратов (со стационарным, движущимся или псевдоожиженным слоем катализатора). Кроме того, сама активность единицы поверхности катализатора зависит не только от его химического состава, но и от способа его приготовления.
Способы повышения содержания железа в железорудных материалах получили название процессов металлизации. Получаемый продукт называют метаялизованным. Под степенью металлизации обычно понимают процентное содержание железа в продукте.
По назначению металлизованные продукты обычно делят на три группы в зависимости от степени металлизации:
1) до 85% Fe -продукт используют в качестве шихты доменной плавки;
2) 85-95 % Fe - продукт используют в качестве шихты при выплавке стали;
3) >98 % Fe - продукт используют для производства железного порошка.
Процессы металлизации железорудных материалов осуществляются при температурах, не превышающих 1000-1200 °С, т. е. в условиях, когда и сырье (железная руда или железорудный концентрат), и продукт представляют собой твердую фазу, а также не происходит размягчения материалов, их слипания и налипания на стенки агрегатов. Такие процессы прямого получения железа из руд получили название процессов твердофазного восстановления (ПТВ). Поскольку получаемый материал напоминает пористую губку, его часто называют «губчатым железом». За рубежом принята аббревиатура DRI (от англ. Direct-Reduced-Iron) или DI (Direct-Iron). Основная масса получаемых продуктов используется в качестве шихты сталеплавильных агрегатов.
Для восстановления оксидов железа в качестве восстановителя обычно используют или уголь (твердый восстановитель), или природный газ (газообразный восстановитель). При этом предпочтительно использование не «сырого» природного газа, а горячих восстановительных газов, так как при этом не затрачивается тепло на диссоциацию углеводородов, а приход тепла определяется нагревом восстановительных газов.
Восстановительные газы получают конверсией 1 газообразных углеводородов либо газификацией твердоготоплива. Конверсия природного газа может быть:
кислородной (воздушной)
СН 4 + 1/2О 2 = СО + 2Н 2 + Q,
СН 4 + Н 2 0 = СО + ЗН 2 – Q,
углекислотной
СН 4 + СО 2 = 2СО + 2Н 2 - Q,
В случае паровой и углекислотной конверсии для протекания реакции требуются затраты тепла. Конверсию осуществляют в специальных аппаратах с использованием катализаторов.
Газификация твердого топлива осуществляется по следующим реакциям:
С + 1/2О 2 = СО + Q,
С + Н 2 О = СО + Н 2 - Q,
С + С0 2 = 2СО - Q,
В настоящее время в мире работает много установок прямого восстановления, главным образом в странах, располагающих дешевым сырьем (Индия, Мексика, Венесуэла, ЮАР).
Существует несколько типов процессов и установок ППЖ (рис. 7.1). Наиболее распространенными являются способы Мидрекс (MIDREX, США) и ХиЛ (HyL, по названию фирмы Hojalata-y-Lamina, Мексика). Способом Мидрекс осуществляется примерно 2/3 всего мирового производства железа прямого получения, способом ХиЛ - примерно ¼
1 От лат. conversio - изменение, превращение
Рис. 7.1. Принципиальные схемы агрегатов
прямого восстановления, используемых в
процессах:
а-Мидрекс (MIDREX); 6-ХиЛ (HyL); е-Круп-па (Krypp-Rennverfahren). Обозначения: О-железорудные окатыши; Р - руда; ГЖ- губчатое железо; ВГ- восстановительный газ; ОТ- отходящий газ; Т- топливо; У- уголь
Главным отличием процесса Мидрекс (рис. 7.2) является способ конверсии природного газа, которая в этом процессе осуществляется диоксидом углерода, содержащимся в отходящем из печи газе, по реакции СН 4 + СО 2 = 2СО + 2Н 2 . Перед подачей отходящего газа в конверсионную установку он проходит очистку от пыли и Н 2 О. Конвертированный газ, содержащий -35 % СО и ~65 % Н 2 , подают в печь при температуре 750 "С. Кроме этого в нижнюю часть печи подают охлажденный оборотный газ. Охлажденные окатыши содержат ~95 % Fe и ~1 % С. Содержание углерода в губке при необходимости может быть повышено.
Металлизованные охлажденные окатыши непрерывно выгружаются в бункер емкостью 5 тыс. т, где хранятся в инертной атмосфере до плавки в дуговых печах. Расход природного газа на процесс составляет около 350 м 3 на 1 т продукта. Этот процесс осуществлен у нас на Оскольском электрометаллургическом комбинате.
Рис. 7.2. Принципиальная схема процесса MIDREX:
1 -воздуходувка; 2 -теплообменник; 3 -смеситель газов; -/-конверсионная установкам-компрессор; 6 -скруббер для колошникового газа; 7-шахтная печь; 8- скруббер-9- вибрационный грохот; 10- брикетный пресс
Основной особенностью процесса восстановления в периодически действующих ретортах ХиЛ (HyL) является применение паровой конверсии природного газа, осуществляемой в аппаратах, в которых расположена кирпичная насадка с добавкой никеля в качестве катализатора. Конверсия протекает по реакции СН 4 + Н 2 0 = СО + ЗН 2 .
Газ перед конверсией подвергается десульфурации. Получаемый конвертированный газ содержит около 14 % СО, 58 % Н 2 , 21 % Н 2 О и 4-5 % СО 2 . Горячий газ проходит через котел-утилизатор и освобождается от паров воды. Сухой конвертированный газ содержит около 73 % Н 2 , 15-16 % СО и 6-7 % СО 2 . Он подогревается до температуры 980-1240 ºС в трубчатых рекуператорах, отапливаемых газом, выходящим из агрегатов восстановления. В этих агрегатах окатыши или руда нагреваются в результате использования физического тепла восстановительного газа и при температуре 870-1050 °С происходит восстановление железа водородом и оксидом углерода. На первых установках в качестве агрегатов восстановления применялись реторты. На установке таких реторт четыре.
Устройство реторты показано на рис. 7.3. Перестановкой реторт с одной позиции на другую обеспечивает ся циклический характер процесса, складывающегося из последовательных
Рис. 7.3. Реторта для металлизации по способу HyL:
1 - гидравлический цилиндр; 2 - тележка; 3 - привод; 4 - кожух; 5- крышка; 6- загрузочная горловина; 7-площадка для обслуживания; 8- резец с рычагами для удаления губки; 9- футеровка; 10- механизм управления откидным днищем; 11 - откидное днище; 12- разгрузочный желоб
операций загрузки, нагрева и восстановления железорудной шихты, охлаждения и выгрузки губчатого железа. После загрузки шихты в реторты в них подают сверху газ. Для выгрузки готовой губки служат резец и специальные разгрузочные скребки. Губчатое железо поступает на желоб и далее на сборный конвейер, транспортирующий губку в сталеплавильный цех. На каждой установке в газовом цикле участвуют четыре реторты, в которых протекают следующие процессы: в одной - предварительный подогрев шихты и восстановление ее газом, выходящим из других реторт, осушенным (без Н 2 О) и подогретым; в двух - довосстановление железа шихты подогретым газом, получаемым в конверсионной установке; в последней - науглероживание.
Степень восстановления железа в готовом продукте составляет 75-92 %. На 1 т продукта (губчатого железа) затрачивают 600 м 3 природного газа и около 36 МДж электроэнергии.
Другие способы получения губчатого железа широкого распространения не получили. Заслуживают внимания лишь технологии, обеспечивающие бескоксовую организацию переработки комплексных руд, содержащих помимо железа такие ценные компоненты, как ванадий, титан, никель и др. Так, например, в Институте металлургии Уральского отделения РАН разработан процесс углетермического восстановления ру-доугольных окатышей при высоких температурах на колосниковых установках с использованием любых некоксующихся углей в качестве твердого восстановителя.
Технологическая схема выглядит следующим образом: 1) окомкование железорудного материала с твердым топливом с получением рудоугольных окатышей; 2) обжиг окатышей на установках колосникового типа с получением высокометаллизованного сырья; 3) использование металлизован-ных окатышей в качестве легирующей присадки при получении стали в электропечах.
Основное количество получаемого методами прямого восстановления ме-таллизованного продукта используют в качестве шихтового материала. Этот продукт имеет ряд отличий от обычно используемой шихты (металлического лома и чугуна).
1. Металлизованный продукт, полученный из чистой шихты, практически не содержит примесей (Cr, Ni, Си, Sn и др.), характерных для обычного металлического лома. Такое ценное качество этого продукта делает его незаменимым сырьем при получении очень чистой стали ответственного назначения.
2. При содержании в продукте 92- 95 % Fe в нем содержится 5-8 % пустой породы (обычно кремнезема и некоторого количества невосстановившихся оксидов железа). При последующей плавке пустая порода переходит в шлак, увеличивая его количество и затраты тепла на его расплавление. Кроме того, для ошлакования кремнезема, содержащегося в пустой породе, требуется дополнительный расход извести, что увеличивает массу шлака еще в большей степени.
3. Получаемый методами прямого восстановления продукт имеет невысокую плотность, поэтому на ряде установок горячий металлизованный продукт подвергают брикетированию, чтобы увеличить его насыпную плотность, использовать металлизованную мелочь, а также чтобы повысить стойкость продукта против вторичного окисления (пассивировать продукт).
Некоторые характеристики метал-лизованного продукта приведены в табл. 7.1.
Таблица 7.1 . Характеристики металлизованного продукта
4. Продукт прямого восстановления часто содержит некоторое количество углерода (в процессе Мидрекс 1-2 %). Это необходимо учитывать при использовании такого материала для производства низкоуглеродистых сталей.
5. Продукт прямого восстановления обычно содержит некоторое количество (<2 %, а иногда и более) оксидов железа. При переплаве такого продукта эти оксиды должны быть восстановлены. Поскольку одновременно с оксидами железа продукт содержит углерод, то при более высоком содержании углерода в продукте допустима наиболее низкая степень металлизации и в связи с этим введено понятие эквивалентная степень металлизации". М ЭКВ = M ф акт + а %С, где М факт - фактическая степень металлизации. Если принять, что в металлизованном продукте окисленное железо находится в виде FeO, то в соответствии с реакцией FeO + С = СО + Fe на 1 маc. долю Fe при восстановлении расходуется 6 маc. долей С, т.е. а = 6 и М экв = М факт + 6 %С. При избытке углерода он расходуется на науглероживание стали. В этих рассуждениях не учтено, однако, что процесс восстановления железа происходит с затратой тепла. Использование продукта прямого восстановления для охлаждения конвертерной плавки показало, что охлаждающее воздействие металлизованного продукта может быть принято в 1,2 раза большим, чем обычного металлического лома.
6. Мелкие кусочки однородной крупности металлизованного материала позволяют организовать высокомеханизированную и при необходимости непрерывную подачу этого материала к сталеплавильным агрегатам.
7. Высокопористый высокометал-лизованный продукт (почти чистое железо) обладает повышенной окисляемостью и пирофорностъю 1 .
При открытом хранении степень металлизации за несколько месяцев и даже недель может снизиться до 70- 90 %. В присутствии влаги окисление сопровождается выделением тепла. Если в закрытое помещение, в котором хранится пирофорный материал, попадет вода, то температура повысится и может произойти возгорание. Приходится учитывать также возможность выделения водорода Fe + Н 2 О = FeO + H 2 , поэтому принимают меры для пассивации металлизованных материалов. Продукты прямого восстановления, учитывая их пирофорность, требуют особых мер предосторожности при хранении и транспортировке.
1 От греч.руг- огонь и pharos - несущий (способность металлов в мелкораздробленном состоянии самовоспламеняться на воздухе).
7.3. «АТОМНАЯ» («ЯДЕРНАЯ») МЕТАЛЛУРГИЯ
Весьма заманчивой является возможность использования в металлургических процессах энергии ядерных реакторов. Имеется ряд предложений и проектов, связанных с реализацией этой идеи. В большинстве из них рассматриваются варианты использования тепла ядерных реакторов для проведения операций твердофазного восстановления. Существуют также предложения использовать атомную энергию для разложения воды с последующим использованием водорода для восстановления железа.
В нашей стране разработана схема ядерно-металлургического комплекса (ЯМК). Предварительные расчеты показали, что использование тепла ядерных реакторов непосредственно для восстановления более эффективно по сравнению с использованием этого тепла на стадии получения восстановительных газов.
В разработанной схеме ЯМК предусмотрены: высокая производительность агрегата, непрерывность процесса, рециркуляция восстановительных газов, так как агрегаты устанавливаются в непосредственной близости от ядерных реакторов. В качестве теплоносителя (от реакторной установки) выбран гелий. Восстановителем выбран природный газ, конвертируемый теплом гелия, нагретого от атомного реактора.
Согласно схеме железорудные материалы должны поступать в шахтную печь, где при температуре около 850 °С произойдет восстановление железа. Полученный продукт предусмотрено использовать в качестве шихтового материала в сталеплавильных печах. По схеме ЯМК отходящие из шахтной печи газы должны очищаться от Н 2 О и СО 2 и многократно использоваться.
Будущее покажет, какой метод использования ядерной энергии в металлургии окажется более эффективным.